di Pierluigi Simonini
L’ Himalayan
La colorazione Himalayan è molto particolare, una cavia di questo colore è tutta Bianca (un tipo di bianco leggermente avorio),fatto salvo per le estremità corporee (anteriore-muso-naso, orecchie nella parte esterna e quattro piedi anche nel plantare) in queste aree compare la pigmentazione del colore a “base”Nera presente nel suo genotipo.
Come abbiamo visto in precedenza, il gene responsabile della colorazione himalayan appartiene alla famiglia dei geni C responsabili della depigmentazione e scoloritura del pigmento rosso, più precisamente dell’allele di tipo recessivo ch.
Essendo un allele recessivo, per manifestarsi e consentire la colorazione himalayan deve presentarsi in forma omozigote (chch), ma avendo come caratteristica quella di depigmentare completamente il colore Rosso, se applicato ad una cavia di questo colore, non consente la pigmentazione delle estremità, tutto il mantello sarà così di colore bianco (non leggermente avorio) e gli occhi saranno pink come sempre accade nel colore himalayan.
Per questo motivo,è auspicabile che una cavia himalayan nel suo genotipo non sia o portatrice di tortie (Eep), o tortie (epep; epe) o ovviamente rossa (ee), perché in qualsiasi parte del corpo fossero presenti le macchie rosse, in particolare se alle estremità, diventando bianche sarebbero motivo di una pezzatura imperfetta.
Quindi come abbiamo visto in precedenza nella tabella dei colori, una cavia Rossa (ee), con gli alleli in omozigosi dell’himalayan (chch), sarà una cavia di colore Pew (bianco ad occhi pink).
Possiamo affermare, che quando ci troviamo in presenza di una cavia Bianca ad occhi Pink, questa potrà essere solo due cose nel suo genotipo: o una cavia Himalayan su base Rossa, o una cavia Rossa ad occhi pink o la sua versione pezzata di Bianco, ma in quest’ultimo caso, solo se abbiamo in abbinamento la presenza dei massimi geni della diluizione del Rosso in omozigosi (crcr).
Riassumendo diciamo che in una cavia Himalayan con la caratteristica colorazione alle estremità, i geni (chch) dovranno essere applicati ad una cavia non rossa, ovvero Nera (E- B-), o Cioko (E- bb), in questi due casi la colorazione himalayan si esprime sufficientemente (Cioko) o al meglio (Nero).
Altre colorazioni più tenui di pigmentazione della famiglia dei neri (lilla, beige, ecc…)sono possibili
nell’himalayan, ma la sfumatura risulterebbe talmente poco evidente da essere quasi o del tutto
impercettibile, quindi insignificante e non corretta.
E’ necessario fare anche una considerazione in merito all’occhio pink della colorazione himalayan: questo tipo di occhio pink non è l’occhio pink espressione dei geni dell’occhio pink (pp), ma bensì il semplice risultato dell’azione del gene del colore himalayan (chch), per questo motivo una cavia himalayan avrà sempre un occhio pink, ma nel suo genotipo può essere un occhio nero in omozigosi (PP) o un occhio nero portatore di occhio rubino (Ppg), o un occhio rubino (pgpg), o veramente un occhio pink (pp).
Quindi se pensiamo che da una cavia Himalayan nascano dei portatori di occhi pink (pp) o pink, se
accoppiata ad una cavia non-himalayan occhi pink, commettiamo un errore.
Queste considerazioni però ci portano a dover fare un’altra affermazione: visto che la colorazione più soddisfacente in himalayan la si ottiene da una cavia geneticamente nera o al più cioko, e non da cavie di “base” lilla o beige ecc….a maggior ragione una cavia himalayan non deve essere nel suo genotipo ad occhi pink, perché in questo caso avremo colorazioni in “base” lilla o beige o comunque troppo chiare per una corretta pigmentazione dell’himalayan.
Possiamo affermare che una cavia himalayan con una colorazione soddisfacente può avere nel suo
genotipo solo occhi neri (P-), o al più rubino (pgpg), in caso contrario non sarebbe sufficientemente
scura di pigmento.
L’Agouti
L’Agouti rappresenta il primo tipo di colorazione presente nelle cavie in natura.
Quando parliamo di Agouti non definiamo un vero e proprio colore nel senso tradizionale del termine, ma generalmente definiamo l’azione di un gene o di una famiglia di alleli dell’agouti che intervengono in due modi:
1. Rendono non uniforme la colorazione di ogni singolo pelo colorandolo diversamente nel corso di tutta la sua lunghezza base-apice (ticked).
2. Organizzano un disegno complessivo nell’intero mantello dell’animale, utilizzando anche diversi tipi di ticked.
ovviamente ciò avviene sulla base degli strumenti e dei colori che il genotipo di ogni singola cavia mette a disposizione.
Torniamo ora al fatto che i colori di “base” nelle cavie sono sostanzialmente due: il Nero e il Rosso o loro “diluizioni”, ed è proprio sulle diverse condizioni e scoloriture di questi colori, sempre presenti nel genotipo di ogni singola cavia, che i geni Agouti applicano la loro azione “utilizzando” ciò che il genotipo mette loro a disposizione, secondo quanto detto ora al punto 1. e al punto 2.
Sintetizzando, possiamo dire che riguardo al punto 1. l’agouti nelle cavie a pelo corto agisce suddividendo la colorazione di ogni singolo pelo in tre parti di varia lunghezza (in quelle a pelo lungo la sequenza raddoppia):
• Base del pelo – Colore presente nel genotipo appartenente alla famiglia del Nero
• Zona intermedia – Colore presente nel genotipo appartenente alla famiglia del Rosso
• Apice del pelo – Colore presente nel genotipo appartenente alla famiglia del Nero
ma a seconda del diverso tipo di gene agouti a cui facciamo riferimento, ciò non viene fatto nel medesimo modo nelle diverse aree del corpo.
Spesso a seconda di come l’agouti si presenta: o in omozigosi o in eterozigosi , differisce la lunghezza della zona intermedia del ticked, conferendo aspetti di colore più “leggero” (omozigosi) o più “intenso” (eterozigosi) al colore del mantello osservato nel suo complesso.
Nelle cavie di colorazione rosso self, la caratteristica colorazione agouti del mantello non può essere evidente (ee sopprime totalmente l’espressione del pigmento a “base” nera e ciò non rende possibile l’alternanza dei due colori tipica del ticked, perché viene a mancare la parte “nera”), ma se la cavia rossa è agouti nel genotipo, trasmetterà questa caratteristica alla prole, e ciò si renderà anche manifesto nel caso sussistano le condizioni perché ciò avvenga (E-; ep-).
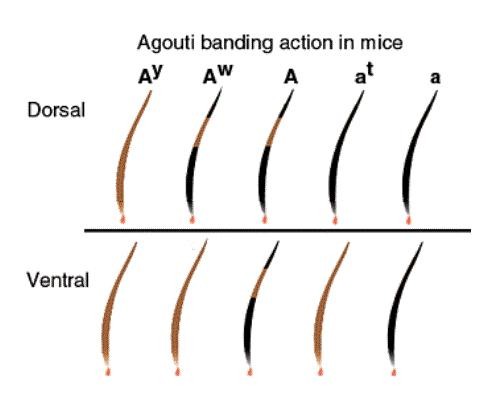
Definiamo ora i diversi tipi di agouti, noi possiamo avere nelle colorazioni delle cavie, quattro tipi di differenti manifestazioni di questo gene:
1. A Agouti Normale
2. ar Solid Agouti
3. at Tan Agouti o più generalmente il Focato (Tan-Otter-Fox)
4. aa Non Agouti (cavia non agouti)
L’ordine col quale sono indicati questi quattro geni dell’agouti è rappresentativo anche dei loro reciproci rapporti di forza e dominanza o subalternità, più precisamente:
il gene dell’agouti normale (A-)è dominante ed è anche il più forte, quando è presente e occupa anche uno solo dei due posti disponibili è sempre manifesto con la sua azione sul colore del mantello quindi tutte le cavie AA; Aar; Aat; e Aa, saranno esteriormente tutte colorate uguali (a parità di caratteristiche di genotipo).
Il gene del solid-agouti ar, è più “debole” di A, ma più “forte” di at e aa, quindi si comporterà come recessivo nei confronti di A (per essere manifesto rispetto ad A, deve passare dalla condizione Aar, alla condizione arar) e dominante nei confronti degli altri due, in particolare una cavia arar; arat o ara sarà sempre solid-agouti in medesima colorazione a parità di caratteristiche del genotipo.
Il gene del colore “focato” at, si comporterà come recessivo nei confronti di A e ar, rispetto ai quali è più “debole”, e come dominante nei confronti di a, quindi il colore di una cavia per essere focato dovrà avere i seguenti alleli: atat o ata.
Il gene del non-agouti è il più “debole” di tutti, ed in quanto tale anche il più recessivo di tutti, lui non “vince” mai su nessuno e per rendere manifesta la sua condizione deve essere presente in omozigosi, ovvero: aa.
Questi quattro geni, con i loro rispettivi rapporti di forza caratterizzano il diverso modo dell’agouti di manifestarsi secondo quanto detto al punto 1. e al punto 2. , condizionando il come e il dove, può e deve esplicarsi l’azione della colorazione agouti.
Possiamo così descrivere le loro azioni:
Agouti Normale (A-)
La colorazione Agouti Normale presenta il “Ticked” a bande su ogni singolo pelo con base del colore della famiglia del nero, zona intermedia con colore della famiglia del rosso e parte apicale con colore sempre della famiglia del nero.
Questo ticked è distribuito in egual modo su tutto il corpo, fatta eccezione dell’area ventrale e palmare dove si modificano i rapporti di lunghezza del ticked: si riduce la parte di colorazione più scura della base, e si allunga leggermente quella a base rossa intermedia che fa scomparire completamente la pigmentazione scura apicale, conferendo un effetto colorazione tinta unita del tipo di tonalità a base rossa presente nel genotipo di quella specifica cavia.
Solid Agouti (arar; ar-)
Nella colore in Solid Agouti, la diversa forma di ticked della zona ventrale e palmare tipica della colorazione Agouti Normale, scompare uniformandosi al ticked presente nel resto del corpo. Scompare il caratteristico effetto “pancia chiara” dell’agouti normale.
Tan Agouti o Focato (atat; ata)
La colorazione Tan Agouti o più genericamente il “Focato”, è una colorazione molto particolare, si presenta con il colore del corpo in tinta unita in base nera (secondo quanto previsto dal genotipo in questione) e una macchiatura della pancia, contorno occhi, naso , mento e parte delle guance, con ticket ad effetto tinta unita appartenente alla famiglia del Rosso (sempre come da genotipo in questione).
Non Agouti (aa)
Il colore Non Agouti rappresenta ovviamente la totale non espressione e mancanza del tradizionale ticket del pelo e quindi della stessa colorazione agouti del mantello.
Tutte le cavie in colorazione self descritte in precedenza ed elencate nelle rispettive tabelle sono Self-non-agouti.
La colorazione di una cavia non-agouti si presenta di tipo self uniforme del colore presente nel suo specifico genotipo (Rossa se rossa, buff se buff, nera se nera ecc…ecc…).
Per ragioni di spazio e per consentire un’esposizione più graduale dei concetti, non ho inserito nelle sequenze dei genotipi delle precedenti tabelle, l’allele del non-agouti in omozigosi (aa) lasciandolo momentaneamente sottinteso e ho fatto la stessa cosa anche con altri geni che vedremo in seguito.
E’ necessario precisare che le possibili combinazioni degli alleli nei genotipi delle colorazioni agouti sono molteplici, ma che non tutte quelle possibili vengono poi ufficialmente riconosciute dalle varie associazioni.
Alcune associazioni e club, ad esempio, ne riconoscono solo sei:
• Goldagouti (Nero e Rosso)
• Lemonagouti (Nero e Crema)
• Silveragouti (Nero e Bianco)
• Orangeagouti (Cioko e Rosso)
• Creamagouti (Cioko e Crema)
• Cinnamonagouti (Cioko e Bianco)
così facendo vengono escluse tutte le loro versioni “diluite” dall’azione di un occhio diverso da quello nero.
In altri casi vengono riconosciute una decina e oltre di colorazioni agouti, ma sta di fatto, che i colori possibili sarebbero anche di più, è inutile aggiungere che oltre le disomogeneità nel riconoscimento di questi colori, spesso medesimi tipi di colorazioni agouti non vengono indicati univocamente con lo stesso nome.
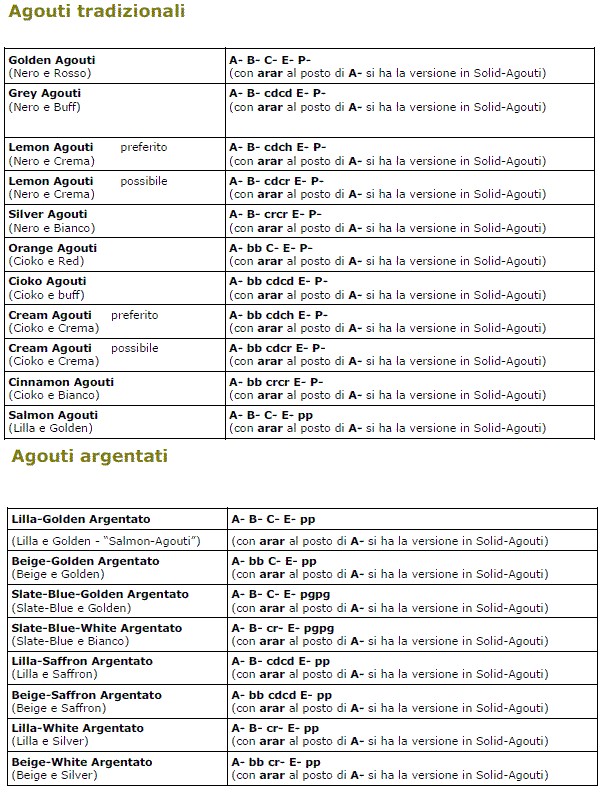
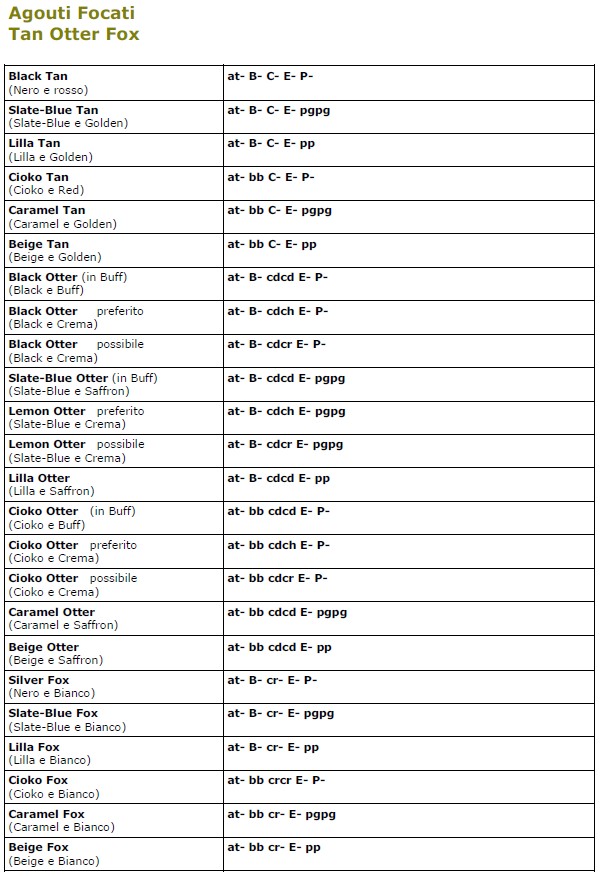
Io di seguito indicherò, aiutandomi con l’uso di tabelle, un elenco dei principali genotipi delle colorazioni agouti per quanto possibile allargata ad un numero più vasto di possibilità.
Saranno indicati come Argentati, le versioni ad occhio Pink di questi colori, ed in taluni casi anche quelle ad occhio Rubino.
Tabelle dei genotipi delle principali colorazioni Agouti
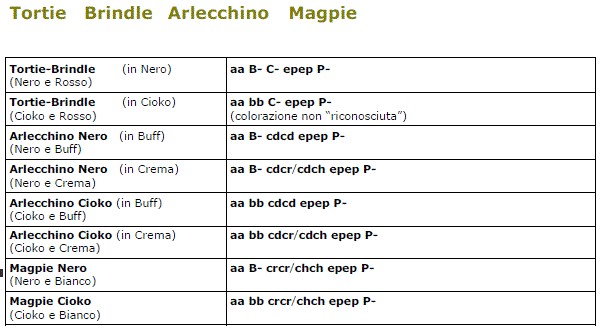
Tortie, Brindle, Arlecchino, Magpie
Riconsideriamo quanto detto nelle prime pagine, in particolare quando parlavamo dei diversi tipi di alleli appartenenti alla famiglia dei geni E (E- ep- e-) detti geni dell’ estensione, che consentono l’espressione rispettivamente del Nero o Cioko (E-), del Tortie o Brindle (ep-) o del Rosso (ee).
Per Tortie o Brindle, intendiamo una cavia in cui il gene (ep-) consente la contemporanea presenza nel mantello di colorazioni a “base” Nera e a “base” Rossa, ma prive dei geni della famiglia C (di scoloritura del colore rosso cd, cr, ch), e più precisamente, secondo le modalità di non-diluizione rappresentate da (C-). Ovviamente è consentita la sua versione in Nero ed in Cioko.
Ciò non toglie, che il gene del colore tortie (ep-) può esplicare la sua azione anche in genotipi dove il Nero ed il Rosso vengono modificati a vario titolo dall’azione delle diluizioni, dell’agouti o di altre colorazioni particolari come ad es. il Roano o il Dalmata.
Abbiamo la colorazione Brindle o un “effetto” Brindle, quando la divisione in pezzature distinte del nero e del rosso, perde di definizione e si ha una “sporcatura” reciproca dei due colori, anche non presente in tutte le chiazze.
Questo effetto detto “brindling”, è poco gradito e penalizzante nelle colorazioni tortie, ma l’esperienza che gli allevatori hanno acquisito nel corso di anni di selezione, insegna che a livello riproduttivo è impossibile eliminare del tutto questo aspetto che di tanto in tanto si ripresenta.
Per ovviare al problema alcuni club hanno accettando questa caratteristica.
Geneticamente parlando, possiamo definire la colorazione Arlecchina una cavia Tortie, ma con i colori Buff o Crema al posto del Rosso, quindi siamo in presenza degli abbinamenti di diluizione del rosso (cdch, cdcr del colore crema o cdcd del colore buff).
A differenza del colore Arlecchino, il Magpie non è altro che una colore Tortie in cui la sua componente Rossa viene schiarita al massimo dai geni cr o ch presenti in omozigosi (crcr; chch), e sotto il loro effetto il colore rosso diventa bianco.
Tutte queste colorazioni possono anche modificarsi sotto l’effetto di un occhio Rubino che modifica il Nero in Slate ed il Cioko in Caramel (pgpg); oppure Pink che modifica il Nero in Lilla ed il Cioko in Beige (pp), ma anche se possibili come colorazioni, rimane da verificare se ad oggi sono “riconosciute” dai vari club.
Lo “Spotting” : il colore Bianco in pezzatura
Lo Spotting non è altro la condizione per la quale possiamo avere in singole pezzature l’abbinamento fra il Bianco e i due principali colori a “base” nera e “base rossa, o distintamente con ciascuno di loro (bianco e nero o bianco e rosso e loro possibili modificazioni) o congiuntamente ad entrambi (tricolori e loro possibili modificazioni).
Il gene dello “Spotting” (bianco in pezzatura), si indica con la lettera S, in particolare possiamo avere due alleli: S (non-spotting) o s (spotting).
S è un gene che ha un comportamento del tutto particolare, ovvero esercita rapporti di “incompleta dominanza” su s .
L’incompleta dominanza di S nei confronti del suo “parzialmente” subordinato s, si può spiegare in questo modo: l’allele S (non-spotting) quando è presente in eterozigosi (Ss), “vince” nei confronti del suo
subalterno non consentendo la presenza della pezzatura in bianco del mantello, ma non “vince” del tutto, infatti s lascia una debole traccia di se colorando di bianco una piccola porzione del mantello, a volte anche solo impercettibilmente con qualche singolo ciuffetto di peli spersi, come semplice testimonianza di se e a dimostrazione che la cavia in questione è portatrice di spotting (bianco pezzato).
Una cavia, relativamente allo spotting, potrà presentarsi nei seguenti modi:
1. SS Non-Spotting (senza tracce di bianco e non portatore di spotting)
2. Ss Non-Spotting (con tracce di bianco e portatore di spotting)
3. ss Spotting (colorazione pezzata di bianco)
Per rendere più complete le tabelle dei genotipi illustrate in precedenza, avremmo dovuto inserire nei genotipi dei colori anche questi possibili modi di presentarsi di S e s, ma per semplificarne la scrittura ciò non è stato fatto.
Ciò non toglie,che possiamo inserire i due alleli S e s nei genotipi indicati nelle tabelle in tutte le loro varianti (diluiti,agouti,roani ecc…) definendo nel nome del colore la dicitura “e Bianco” o “Self” o “Minimum Bianco” a seconda che si presentino rispettivamente (ss) o (SS) o (Ss).
Con SS abbiamo tutte le colorazioni Self-Colour e Tortie pezzate correttamente e prive di fiammelle bianche macchie più o meno grandi.
Con Ss abbiamo tutte le colorazioni in Self-Colour e Tortie pezzate in modo non propriamente corretto (minimum bianco), ovvero con la classica presenza di piccole macchie bianche (carrier Spotting).
Con la presenza di ss abbiamo tutti quei colori Spotting che se abbinati a E- ci danno il Bianco/Nero, se abbinati a ee il Bianco/Rosso e se abbinati a ep- i tricolori o Tortie/White e ovviamente loro versioni diluite o in agouti o entrambe le cose.
Quando siamo in presenza di ss le macchie Bianche presenti sul mantello possono variare per regolarità e posizione, per quantità e grandezza e per nettezza.
I vari standard di definizione delle colorazioni spotting, tendono più o meno tutti a prediligere la maggiore regolarità geometrica della pezzatura, la nettezza delle macchie, e in alcuni colori come ad es. il Dutch (ss olandese) a indicare la precisa collocazione delle macchie stesse.
La difficoltà con lo Spotting, sta nel fatto che diversi studi hanno dimostrato che meno della metà dell’ereditarietà del tipo di pezzatura è di tipo “geneticamente prevedibile” a causa dell’interferenza di geni modificatori che alterano l’ereditarietà della pezzatura stessa, anche quando accoppio soggetti con caratteristiche di pezzatura “corretta” o molto simili.
Con lo Spotting ci troviamo sempre di fronte ad una percentuale assolutamente non trascurabile di “random effect” cioè la casualità degli effetti sulle marcature mentre l’embrione si sta sviluppando nonostante le caratteristiche dei genitori.
Ciò nonostante, selezionando ed accoppiando soggetti con colorazioni bilanciate e regolari, in particolare se riferite a colorazioni particolarmente “difficili” come ad esempio il Dutch, è innegabile che aumentiamo le probabilità di avere nella prole soggetti con pezzature per quanto possibile corrette e regolari.
Il Dutch ad es. è una colorazione Spotting che si deve presentare solo in un determinato modo, ovvero, la parte colorata del mantello deve includere tutta la zona posteriore sino al costato inferiore alla quale deve seguire una pezzatura bianca a “cintura che includa le zampe anteriori per poi risalire con un disegno a “V rovesciata” nella zona mento-naso-frontale e sino alla zona cervicale lasciando al colore le restanti parti dx e sx della testa.
Un ulteriore tipo di colorazione Spotting particolarmente “difficile” è il Belted in questa colorazione è richiesto che l’unica pezzatura Bianca si presenti sotto forma di macchia circolare detta a “cintura” collocata nella parte del corpo compresa fra le zampe anteriori e posteriori, conferendo il caratteristico effetto di “indossare” una cintura di colore bianco.
Noi però, non riusciamo ad indicare nei genotipi dei colori Spotted i geni minori e le loro variabili che consentono l’espressione di questi ultimi due tipi di pezzature, possiamo solo indicare i genotipi che identificano lo Spotting nelle sue forme più generiche (bicolori, tricolori ecc.).
Black-White Spotting | aa B- C- E- P- ss |
Red-White Spotting | -/- -/- C- ee P- ss (-/- = ininfluente la presenza di A- o B-) |
Tortie-White Spotting | aa B- C- epep P- ss |
(applicando ss a tutti i colori possibili non elencati in questa tabella, otteniamo le restanti versioni | |
Dalmata&Roano
Il Dalmata ed il Roano sono due colorazioni molto particolari, sicuramente molto belle e d’effetto, ma i due geni che le generano, se presenti in omozigosi diventano letali o causa di problemi molto gravi.
Per questo motivo assume estrema importanza la loro conoscenza e la piena consapevolezza delle problematiche che possono causare se presenti congiuntamente, o in omozigosi nel genotipo.
Dalmata
Nella cavia Dalmata il colore è distribuito in modo del tutto particolare: la pigmentazione più intensa la troviamo nei piedi e nella testa ove è presente anche una macchia bianca, solitamente a forma di “V” rovesciata nella zona naso-frontale (più o meno come nel Dutch), mentre il resto del corpo è di colore bianco, ma ricoperto da una rada maculatura costituita da piccole macchie pigmentate.
Il gene responsabile di questa caratteristica colorazione si chiama Wh (dalmata), mentre indicheremo con wh (non-dalmata) il suo allele antagonista.
Wh si comporta da incompleto dominante nei confronti di wh
Possiamo avere i seguenti abbinamenti nello specifico locus di Wh:
1. WhWh Condizione letale o causa di gravi problemi
2. Whwh Colorazione Dalmata
3. whwh Colorazione Non-Dalmata
Nel primo caso (WhWh) possiamo avere cavie bianche, a volte prive di bulbi oculari o con bulbi oculari di ridotte dimensioni e funzionalità ridotta, cecità e sordità, ma nella stragrande maggioranza dei casi questa condizione è letale e molto spesso i piccoli vengono “riassorbiti” in fase di gestazione.
Nel secondo caso (Whwh) abbiamo la classica colorazione Dalmata descritta in precedenza. E’ necessario precisare che vi sono anche dei geni minori che determinano l’ereditarietà di una bella e “corretta”pezzatura Dalmata.
Nel terzo caso (whwh) non ci troviamo in presenza di una colorazione Dalmata e la cavia sarà del colore indicato nel suo genotipo, ma può essere portatrice o non portatrice dei geni minori che determinano una bella colorazione Dalmata.
Back Dalmata | aa E- B- C- P- SS Whwh |
Cioko Dalmata | aa E- bb C- P- SS Whwh |
[*] per ottenere gli altri colori Dalmata e rispettivi genotipi basta inserire (Whwh) nei diversi | |
Ovviamente per evitare di ricadere nel primo caso (WhWh), con tutto quello che ne conseguirebbe, chi alleva Dalmata è “costretto” ad accoppiare Dalmata (Whwh) con non-Dalmata (whwh), possibilmente in colorazione self e preferibilmente su “base” nera, i piccoli generati da questi accoppiamenti “teoricamente” potranno essere per il 50% Dalmata e per il restante 50% non-Dalmata.
Così facendo, da un lato evitiamo tutti gli aspetti pericolosi di questo gene, ma dall’altro non sapremo quali cavie self non-Dalmata ottenute da questi accoppiamenti sono portatrici anche dei geni minori che determinano una pezzatura più corretta del Dalmata, rendendo poi più difficile capire quali di queste cavie è più conveniente reinserire in riproduzione nello specifico programma di allevamento.
Un altro particolare aspetto del gene Wh è quello che sembra avere la capacità di inibire e condizionare la produzione del pigmento rosso in particolare nella zona ventrale, riducendo di fatto le “potenzialità” espositive di determinate colorazioni di cavie.
Roano
Nella cavia Roana il mantello è oggetto di una forte brizzolatura in tutto il corpo fatta eccezione della testa dove il colore di “base” della cavia si può esprimere liberamente nella sua forma naturale non condizionata.
Il gene responsabile di questa colorazione si chiama (Whmi), si comporta da dominante nei confronti del suo allele antagonista wh (non-Roano, che è lo stesso allele non-Dalmata perché gli alleli del Roano e del Dalmata stanno sullo stesso locus genico)).
Possiamo avere i seguenti abbinamenti nello specifico locus di (Whmi) [*]:
1. WhmiWhmi Condizione letale o causa di gravi problemi
2. Whmiwh Colorazione Roana
3. whwh Colorazione Non-Roana
Nel primo caso (WhmiWhmi) possiamo avere una condizione letale, oppure delle cavie tutte bianche con la presenza di “micro-oftalmia” (occhi piccoli), scarso sviluppo, generale debolezza, sterilità (ma non sempre), morte precoce (ma non sempre).
Nel secondo caso (Whmiwh) avremo la classica colorazione Roana.
Nel terzo caso (whwh) non abbiamo una colorazione Roana e la cavia esprimerà la colorazione presente nel suo particolare genotipo.
Black-Roan | aa E- B- C- P- SS Whmiwh |
Cioko-Roan | aa E- bb C- P- SS Whmiwh |
[*] per ottenere gli altri colori roani e rispettivi genotipi basta inserire (Whmiwh) nei diversi | |
Ovviamente per evitare di ricadere nel primo caso, come per quanto visto per la colorazione Dalmata, che alleva Roani è “costretto” ad accoppiare Roani (Whmiwh) con non-Roani (whwh), preferibilmente in colorazione self, anche se colorazioni su “base” spotting in tricolore risultano particolarmente belle.
Si tende a scoraggiare l’abbinamento spotting e Roano onde evitare che un eccesso di pezzatura bianca dovuta allo spotting, renda difficile il riconoscimento della contemporanea presenza della colorazione
roana.
Questa condizione aumenterebbe i rischi di incorrere a nostra insaputa in accoppiamenti fra roani, lo stesso ragionamento vale anche se riferito a tutti quei colori come ad es. l’himalayan capaci di mascherare nel fenotipo della cavia la presenza delle colorazioni Roane e Dalmata.
[*] con riferimento alla bibliografia di questo articolo, il prof. Sewell Wright, ipotizzava che la colorazione roana fosse dovuta ad un gene (si) di tipo recessivo che sotto l’azione di un suo “modificatore” determinasse la colorazione Roana. Ad oggi però, risulta innegabile il comportamento dominante del gene responsabile del roano comunemente identificato con (Whmi) quindi i due geni non possono essere la stessa cosa, molto probabilmente (si) è imparentato o è il gene responsabile di una brizzolatura o “argentatura” che si estende anche alla pigmento colorato della testa tipica dell’effetto “silvering” o “silberling” o comunque lo si possa chiamare.
Teoricamente noi possiamo trovarci anche in presenza di una cavia che è contemporaneamente Dalmata e Roana, poiché il loro allele antagonista (wh) e locus genico è lo stesso i due rispettivi alleli dominanti possono trovarsi abbinati nello stesso locus ed esercitare entrambi la loro azione contemporaneamente secondo la sequenza (WhmiWh), in questi casi avremo una cavia di colore bianco, debole, con problematiche evidenti quali scarso accrescimento, problemi oculari, possibili sordità ecc…in linea con quanto avviene nei casi non immediatamente letali delle omozigosi del Dalmata e del Roano.
Sabbia (sable)
Il colore Sabbia, più che un colore vero e proprio, rappresenta uno di quei casi in cui un carattere recessivo del genotipo influenza il fenotipo della cavia rendendo parzialmente evidente l’effetto che avrebbe se fosse in grado di condizionare il colore e manifestarsi.
Fenotipicamente una cavia color Sabbia non è altro che una cavia di colore preferibilmente scuro appartenente alla “famiglia” del Nero, che mette leggermente in evidenza una pigmentazione ancora più scura nelle medesime posizioni in cui si pigmenterebbe se fosse di colore himalayan.
In questo specifico caso il responsabile di tutto ciò è l’allele (ch) che in omozigosi genera il colore himalayan (solo se applicato ad un colore appartenente alla “famiglia” del colore Nero E-).
Detta in parole povere i colori Sabbia, vengono espressi da tutte quelle cavie a “base” nera (E-) che sono al contempo carrier Himalayan, ovvero hanno l’allele (ch) abbinato ad un altro allele della famiglia (C-).
Quindi i colori sabbia potranno presentare nel locus degli alleli (C-) i seguenti abbinamenti: (Cch); (cdch); (crch), sarà sempre presente (ch) in forma eterozigote proprio perché stiamo parlando di una cavia carrier himalayan.
A seconda che questa particolare caratteristica venga abbinata ai vari genotipi delle di “base” nera, possiamo avere il Black-Sable, il Cioko-sable, Lilla-Sable, Beige-Sable, Slate-Sable, Caramel-sable ecc.
Nella tabella di seguito scriverò solo i principali, gli altri colori e genotipi sono facilmente intuibili dalla prima tabella delle colorazioni self, considerando tutti i colori con (E-) in cui sia possibile avere (-ch), inserendo il suffisso “Sable” al nome del colore.
Black-Sable | aa E- B- Cch P- SS whwh rnrn [*] |
Slate-Sable | aa E- B- Cch pgpg SS whwh rnrn |
Cioko-sable | aa E- bb Cch P- SS whwh rnrn |
Lilla-Sable | aa E- B- Cch pp SS whwh rnrn |
Beige-Sable | aa E- bb Cch P- SS whwh rnrn |
[*] in questi genotipi ho indicato i possibili abbinamenti nel locus di (C-) abbinando sempre | |
Bibliografia
Cavy Genetics by Peter and Cell Herman
Basic Color Genetics by Pip Squeak Caviary
Cavy Genetics: An Explorations by Nick Warren
Colour Genetics of the Cavy by Catherine Whiteway (alla sezione Cavy Colors)
Genetic aspects of pigment production in the guinea pig1
by Mary T. Harman and Annette Alsope Case
Accoppiamenti Ammessi e Consigliati
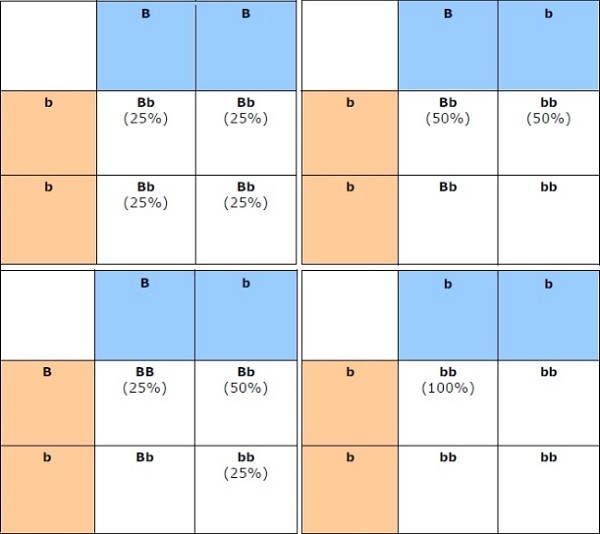
Peruviana è dominante AT = Alpaka recessivo
Peruviana X peruviana = 100% peruviane
Peruviana X Alpaka = 100% peruviane portatori AT
Peruviana (AT) X peruviana (AT) = 50% peruviane 25% alpaka 25% peruviane (AT)
Peruviane (AT) X Alpaka = 50% peruviane (AT) e 50% alpaka
Alpaka x alpaka = 100% alpaka
_____________________________________________________
Coronet è dominante SH = Sheltie MT=Merino TX=Texel sono recessivi
Coronet X coronet = 100% coronet
Coronet X sheltie = 100% Coronet portatori SH
Coronet (SH) x Coronet (SH) = 50% coronet, 25% sheltie e 25% coronet (SH)
Coronet (SH) X sheltie = 50% coronet (SH) e 50% sheltie
Sheltie X sheltie = 100% sheltie
Coronet X merino = 100% coronet (MT)
Coronet (MT) X merino = 50% coronet e 50% merino
Coronet (MT) X coronet (MT) = 50% coronet, 25% merino e 25% coronet (MT)
Merino X merino = 100% merino
Coronet X texel = 100% Coronet (TX)
Coronet (TX) X texel = 50% coronet (TX) e 50% texel
Coronet (TX) X coronet (TX) = 50% coronet , 25% texel e 25% coronet (MT)
Texel X texel = 100% texel
Merino X sheltie = 100% coronet
Merino (SH) X sheltie = 50% coronet e 50% sheltie
Merino (SH) X merino (SH) = 50% merino, 25% sheltie e 25% coronet
Sheltie X texel = 100% sheltie
Sheltie (TX) X texel = 50% sheltie (TX) e 50% texel
Sheltie (TX) X sheltie (TX) = 50% sheltie, 25% texel e 25% sheltie (TX)
Texel X texel = 100% texel
Merino X Texel = 100% merino
Merino (TX) x Texel = 50% merino e 50% texel
Merino (TX) X Merino (TX) = 50% merino, 25% texel e 25% merino (TX)
___________________________________________________
Americana dominante US Teddy recessivo
Americana X americana = 100% americane
Americana X US Teddy = 100% americane (US Teddy)
Americane (US Teddy) X americana (US Teddy) = 50% americane,
25% US Teddy, 25% americane (US Teddy)
US Teddy X US Teddy = 100% US Teddy
Pierluigi Simonini – Vice presidente ANAC
 | L’ANAC promuove la diffusione delle cavie domestiche (Cavia porcellus), incoraggia l’allevamento, lo studio e il miglioramento delle diverse razze. Cura inoltre la tenuta dei Libri Genealogici delle cavie di razza, e degli altri elenchi eventualmente necessari al corretto raggiungimento degli scopi sociali, in armonia con le norme nazionali e dell’UE. http://www.agraria.org/cavie/anac.htm |
 | Voglio una Cavia Acquista online >>> |